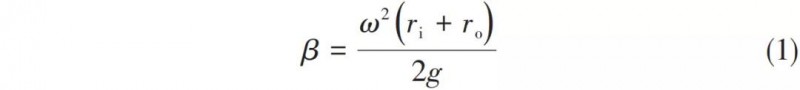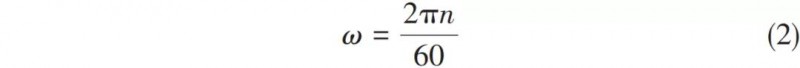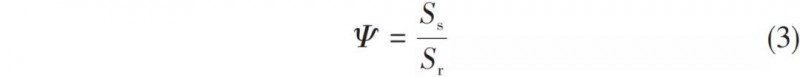超重力反应结晶碳化法制备球形碳酸钙
 2021-12-19
5800
2021-12-19
5800核心提示:超重力反应结晶法在碳酸钙制备中具有强化传质作用、产品粒度分布窄等优点。本文以高浓度氢氧化钙浆液作为原料,氯化铵与L-谷氨
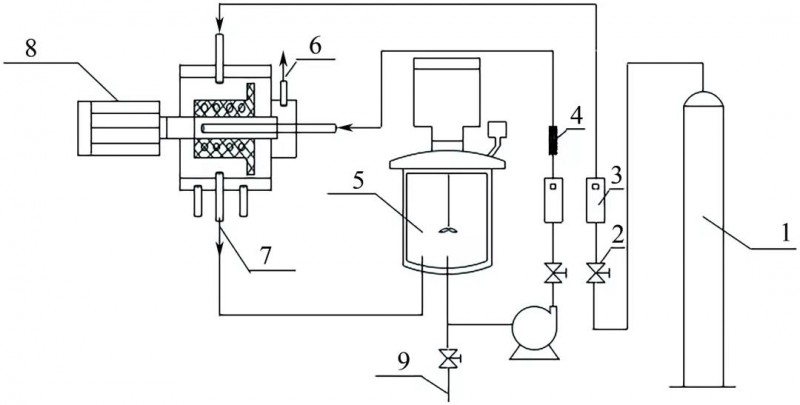
超重力反应结晶法在碳酸钙制备中具有强化传质作用、产品粒度分布窄等优点。本文以高浓度氢氧化钙浆液作为原料,氯化铵与L-谷氨酸为添加剂,使用超重力反应器成功制备粒径分布较为均匀、形貌较为规整的球形碳酸钙。探究了各因素在超重力反应结晶法制备碳酸钙中的影响,通过改变添加剂的量与超重力因子等考察球形碳酸钙的最佳制备条件。采用扫描电子显微镜(SEM)、X射线衍射(XRD)、傅里叶变换红外光谱仪(FTIR)和静态颗粒图像分析等测试手段对碳酸钙产物进行分析,并通过在反应过程中抽样测试的方法探究反应全过程中添加剂对碳酸钙的影响。结果表明,所制备的碳酸钙为粒径约500nm、晶型为球霰石的球形碳酸钙,同时在L-谷氨酸和氯化铵添加量分别为氢氧化钙质量的4%与20%、超重力因子为161.0的条件下所制备的球形碳酸钙形貌最为规整。碳酸钙作为一种优质填料和白色颜料,广泛应用于众多化工行业。碳酸钙常见的形态主要有无规则形、纺锤形、球形、片形和立方体形等,不同形态的碳酸钙其应用领域和功能各不相同,其中,球形碳酸钙凭借良好的分散性、流动性、溶解性及比表面积大等特点,在塑料、橡胶、食品与造纸等领域有着重要的应用。目前球形碳酸钙主要制备方法有复分解法和碳化法。复分解法虽可制得形貌规整、分散度好的球形碳酸钙,但这种方法原料较贵且会引入大量的杂质离子,不适合工业化生产。碳化法是工业上最为常用的方法,传统碳化法主要分为间歇式碳化法与连续喷雾式碳化法。虽然碳化法的成本较低,可以进行大规模生产,但传统碳化法制备球形碳酸钙存在粒径分布不均匀、生产效率低等问题。超重力反应结晶法是一种新型的制备纳米材料的方法,其本质是通过高速旋转产生巨大离心力,模拟出超重力场的环境。超重力反应器内高速旋转的填料转子将液体打成液丝、液滴或液膜,液体比表面积急剧增大,与此同时快速更新相界面,相间的传质速率比传统塔器设备高出1~3个数量级,微观混合和传质过程得到极大强化,故反应时间相比于传统碳化法缩短了,产品具有粒度小、粒径分布窄、产品纯度高、形貌更为规整等优点。超重力反应器由于良好的微观混合和传质效果,被广泛地应用于纳米材料的制备。北京化工大学超重力工程研究中心的陈建峰等成功合成了粒径分布窄、形貌规整、长径比较高(12~20)的碳酸钙晶须。但有关超重力反应器制备球形碳酸钙的报道甚少。目前有报道在超重力环境中,以天冬氨酸作为晶型控制剂,乙醇与水混合作为反应溶剂生成球形碳酸钙,但其存在部分原料成本价格偏高、所制备球形碳酸钙晶型不均一、产物为方解石与球霰石等问题。球形碳酸钙在多数情况下是由球霰石生长而成的,因此制备出纯净的球霰石晶体对球形碳酸钙的制备有重要意义。球霰石作为热力学上不稳定的晶型,在潮湿环境与水溶液中难以稳定存在,需要使用一些特殊的方法才能稳定获得。研究表明在碳化反应过程中引入NH4+不仅可以在结晶过程中抑制方解石的生成,向利于碳酸钙晶型往球霰石方向转变,而且NH4+的氛围又能够使生成的球霰石在溶液中稳定存在。与NH4+不同的是,酸性氨基酸在溶液中会发生解离并与Ca2+结合形成晶种模板,在晶种模板的影响下也会使得生成的碳酸钙出现亚稳态晶相,并且合适的氨基酸的引入会在碳酸钙结晶过程中产生特定的功能并对形貌进行修饰。本文将使用价格低廉的谷氨酸与氯化铵作为添加剂,研究在超重力场中球形碳酸钙的可控制备,并考察两种添加剂在碳酸钙合成中的作用。石灰石(CaCO3),崇左南方水泥有限公司,CaCO3质量分数97%。生石灰(CaO),工业级,实验室自主制备。CO2,99.5%,钢瓶气体,广西诚信气体研究有限公司。L-谷氨酸(C5H9NO4),分析纯,南宁蓝天实验设备有限公司。氯化铵(NH4Cl),分析纯,南宁蓝天实验设备有限公司。实验装置流程如图1所示,其内部重要参数如表1所示。
图1 超重力反应结晶实验装置
1—CO2气体钢瓶;2—阀门;3—流量计;4—pH计;5—循环料液釜;6—排气口;7—液体出口;8—旋转填充床;9—出料口
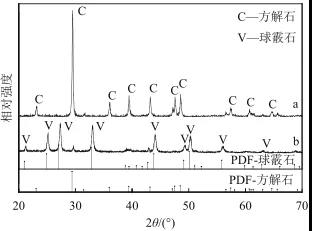
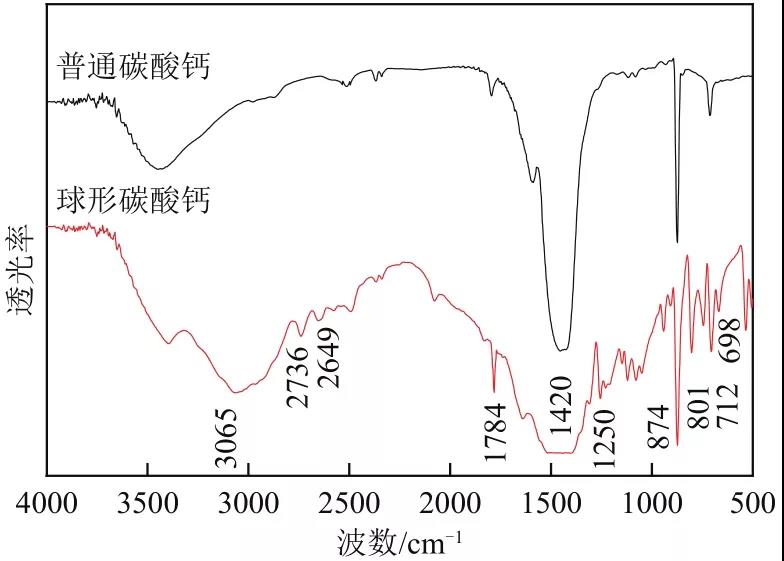
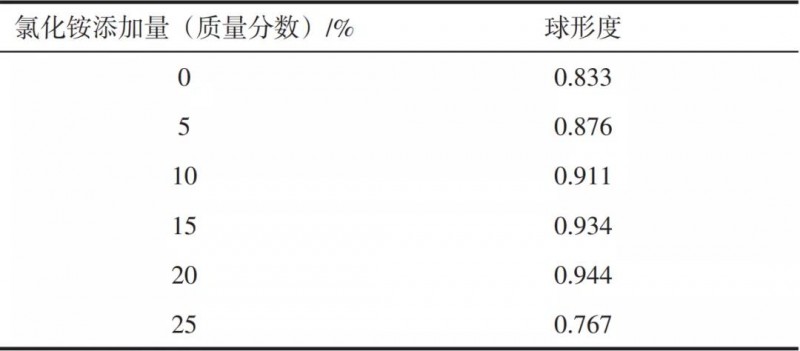
超重力因子是旋转填料床的平均超重力加速度与重力加速度之比,为量纲为1量,用来描述旋转填料床中超重力场的强度,按式(1)、式(2) 计算。式中,β为超重力因子;ω为角速度,s-1;ri为转子填料内半径,m;ro为转子填料外半径,m;g为重力加速度,取g=9.8m/s2;n为超重力机转速,r/min。相比于文献中的设备,本文移除了设备自带的循环水箱而采用大功率外接循环水,对温度的控制更加稳定。先将石灰石在1100℃条件下进行煅烧,加入水配制成氢氧化钙浆液,经200目过筛去除残渣,调浓,并陈化不少于24h,加入L-谷氨酸与氯化铵进行混合,移入循环料液釜当中,氢氧化钙浆液在泵的作用下进入旋转填充床中,经由液体分布器的作用喷向填料转子,填料转子高速旋转向填料外缘流动,CO2从气瓶进入到填料床当中,由填料外缘向内缘流动,气液两相发生逆流接触进行碳化反应生成碳酸钙。此后原料中未反应的Ca(OH)2和生成的碳酸钙浆液一同回流至循环料液釜中搅拌混合均匀,再循环重复以上碳化过程,直至料液的pH降至7时反应结束。从出料口收集碳酸钙浆液。经过洗涤、离心、干燥等步骤后,得到碳酸钙成品。扫描电子显微镜(SEM),S-3400N,日本Hitachi公司。工作电压15kV,表征晶体形貌。高真空环境,在不导电的晶体表面镀一层金薄膜,通过这层与样品表面起伏一致并不改变样品表面二次电子信号的导电膜,获得微观晶体形貌。X射线双晶粉末衍射仪(XRD),Smartlab-9kW,日本理学公司。Cu Kα靶,工作电压为40kV,电流40mA,步长0.03°,扫描速率10°/min,衍射角范围20°~90°。XRD检测的样品是碳酸钙粉末,使用玻璃片将其平铺于载玻片的凹槽当中,将载玻片置于仪器当中进行分析。静态颗粒图像分析仪,MORPHO1OGIG3S型,马尔文仪器有限公司。将碳酸钙样品分散于乙醇中,滴于载玻片上进行干燥,置入仪器中进行球形度拟合测定,球形度用于衡量一个物体的球形化程度,在1935年,由Wadell定义,定义为式(3)。式中,Ψ为球形度,球形度为表征颗粒形貌的参数,形貌上越接近球的颗粒,其球形度越接近于1;Ss与Sr分别为理想球体的表面积和该物体实际表面积。傅里叶变换红外光谱仪(FTIR),Nicolet iS50,美国Thermo Fisher公司。对碳酸钙样品进行表征,考察碳酸钙内部的官能团与化学键。测试方法为KBr压片法,扫面范围400~4000cm-1,分辨率2cm-1,扫面次数20次。图2为在L-谷氨酸和氯化铵添加量分别为氢氧化钙质量的4%和20%、超重力因子为161.0的条件下制备的球形碳酸钙的SEM图。从图中可以看出,在碳化过程中添加L-谷氨酸和氯化铵制备出的碳酸钙粒子形貌为球形,产品大小比较均一,形貌较好,从放大图中可以看到所制备的球形碳酸钙表面并不光滑,是由更小的纳米粒子聚集而成。图3中a、b分别为不添加L-谷氨酸与氯化铵和添加L-谷氨酸与氯化铵所制备得到碳酸钙的XRD图。通过分析可知,当不添加L-谷氨酸与氯化铵时,所制备的碳酸钙为方解石晶型且具有较高的纯度。当体系中引入L-谷氨酸与氯化铵时,碳酸钙晶型为球霰石型且方解石晶相并未出现。可以认为L-谷氨酸与氯化铵的引入不仅使碳酸钙的形貌发生改变,而且改变了碳酸钙的晶型,使碳酸钙以不稳定的球霰石晶型存在。分别对不添加L-谷氨酸与氯化铵和添加L-谷氨酸与氯化铵所制备的碳酸钙进行红外分析得到图4。从图4中可以看出,不加入添加剂的普通碳酸钙在1784cm-1处存在C=O伸缩振动峰,1420cm-1存在C―O伸缩振动峰,874cm-1处存在CO32-面外弯曲振动峰,712cm-1处存在O―C―O的面内弯曲振动峰,而引入添加剂制备得到的球形碳酸钙与之相比,增加了3065cm-1处的O―H伸缩振动峰、2736cm-1处的C―H伸缩振动峰、2649cm-1处O―H伸缩振动峰、1250cm-1处O―H面内弯曲振动峰、801cm-1处伯胺N―H面外弯曲振动峰以及698cm-1处C―H面外弯曲振动峰。根据这些基团,可以确定球形碳酸钙中存在L-谷氨酸。分别对不添加L-谷氨酸与氯化铵和添加L-谷氨酸与氯化铵所制备的碳酸钙进行红外分析得到图4。从图4中可以看出,不加入添加剂的普通碳酸钙在1784cm-1处存在C=O伸缩振动峰,1420cm-1存在C―O伸缩振动峰,874cm-1处存在CO32-面外弯曲振动峰,712cm-1处存在O―C―O的面内弯曲振动峰,而引入添加剂制备得到的球形碳酸钙与之相比,增加了3065cm-1处的O―H伸缩振动峰、2736cm-1处的C―H伸缩振动峰、2649cm-1处O―H伸缩振动峰、1250cm-1处O―H面内弯曲振动峰、801cm-1处伯胺N―H面外弯曲振动峰以及698cm-1处C―H面外弯曲振动峰。根据这些基团,可以确定球形碳酸钙中存在L-谷氨酸。为研究氯化铵添加量对碳酸钙结晶的影响,选定L-谷氨酸添加量为氢氧化钙质量的4%,超重力因子为161.0,改变氯化铵添加量为氢氧化钙质量的0、5%、10%、15%、20%、25%。其氯化铵添加量对碳酸钙形貌与晶型影响分别如图5与图6所示,对碳酸钙球形度测试得到结果如表2所示。从图5可见,在不加入氯化铵的情况下制备的碳酸钙为类球形,球形度很低,仅存在部分类球形碳酸钙,这是由于氢氧化钙的浓度过高,颗粒团聚严重所致。随着氯化铵的引入,碳酸钙逐渐转变为规则的球形,当氯化铵添加量为20%时,形貌最为规整,而当氯化铵添加量进一步升高至25%时,碳酸钙形貌被破坏,多数成长为团聚的大块。
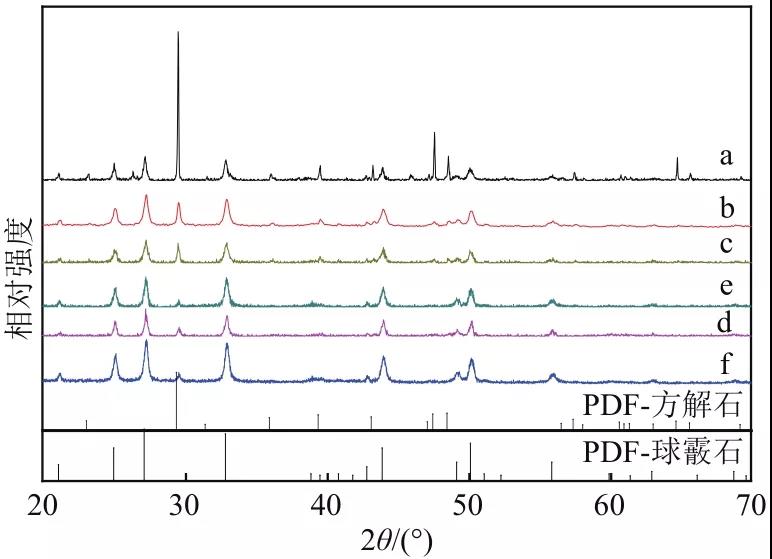
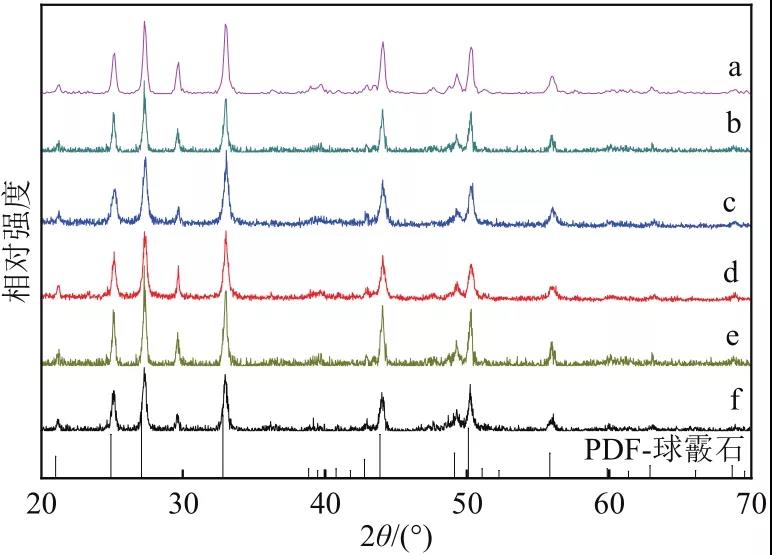
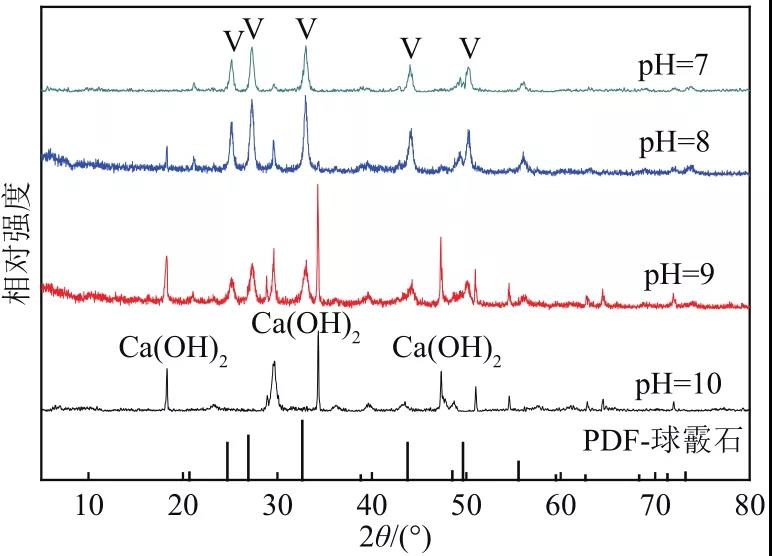
图6 不同氯化铵添加量下所制备的碳酸钙XRD图
a—0;b—5%;c—10%;d—15%;e—20%;f—25%
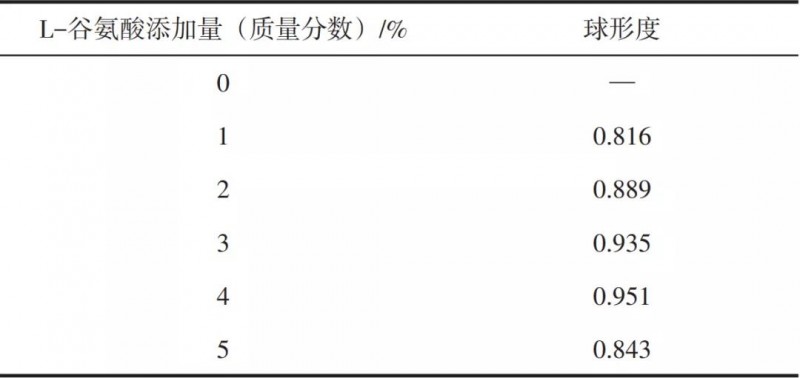
从表2球形度测试结果可以得出与SEM图相一致的结果,不加入氯化铵时碳酸钙球形度较低,为0.833,随着氯化铵的不断加入,所得球形碳酸钙的球形度逐步提高,并在氯化铵添加量为氢氧化钙的20%时达到0.944的最高点。而当氯化铵加入量进一步提升,碳酸钙球形度下降至0.767。从图6可知,未加入氯化铵时,体系中出现了球霰石晶相,且随着反应的进行,球霰石并未转变为热力学上更稳定的方解石,证明谷氨酸作为酸性氨基酸在碳化反应中对碳酸钙的晶型形成存在影响。随着铵离子的引入,铵离子在溶液中对球霰石转变为方解石这一反应进行了抑制,在XRD中表现为方解石晶相消失,碳酸钙全部成长为球霰石,这一晶型的碳酸钙在L-谷氨酸的修饰下最终成长为球形碳酸钙。为研究L-谷氨酸添加量对碳酸钙结晶的影响,选定氯化铵添加量为氢氧化钙质量的20%,超重力因子为161.0,改变L-谷氨酸添加量为氢氧化钙质量的0、1%、2%、3%、4%、5%。L-谷氨酸添加量对碳酸钙形貌与晶型影响分别如图7与图8所示,其碳酸钙球形度测试结果如表3所示。从表3分析可知,当不加入L-谷氨酸时,碳酸钙并不成球,随着L-谷氨酸的不断加入,碳酸钙球形度不断升高,当添加量为4%时,球形度最高为0.951,但当L-谷氨酸加入过多,同样会使得原本规整的球形碳酸钙转变为团聚的大块,这与图7中SEM图反映出的碳酸钙球形貌变化相一致,说明谷氨酸的加入对碳酸钙的形貌具有修饰作用。从图8分析可知,因溶液中存在较高浓度的NH4+,NH4+的存在使得球霰石优先形成并抑制球霰石向热力学上更稳定的方解石转变,富含NH3与NH4+的溶液体系能够使得球霰石这种原本不稳定的晶相稳定存在于溶液中,故体系中生成的碳酸钙均为纯净的球霰石。
图7 不同L-谷氨酸添加量下所制备的碳酸钙SEM图
图8 不同L-谷氨酸添加量下所制备的碳酸钙XRD图
a—0;b—1%;c—2%;d—3%;e—4%;f—5%
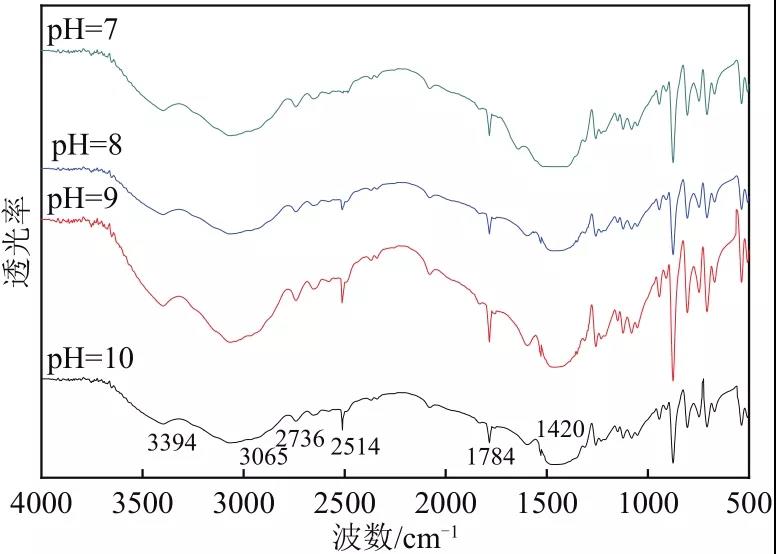
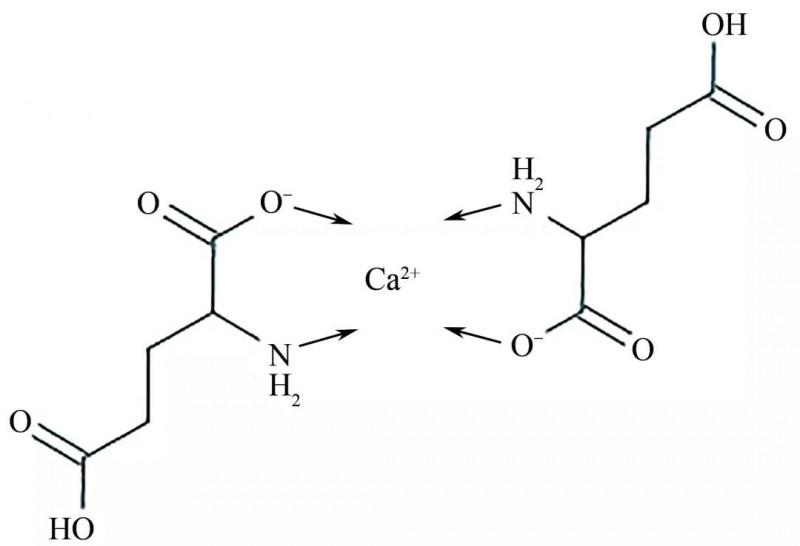
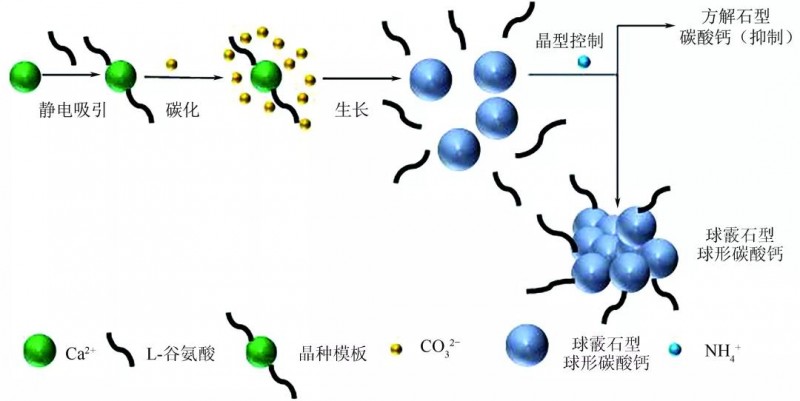
为研究超重力因子对碳酸钙结晶的影响,分别选定L-谷氨酸和氯化铵添加量为氢氧化钙质量的4%和20%,改变超重力因子为40.2、71.5、111.7、161.0和219.1。超重力因子对碳酸钙形貌的影响如图9所示,碳酸钙球形度测试结果如表4所示。由图9和表4可见,当超重力因子为40.2时,碳酸钙结晶的球形度最低,随着超重力因子不断提高,碳酸钙结晶的球形度也随之增大,但当超重力因子为219.1时,碳酸钙结晶的球形度开始下降。超重力因子大小的控制是通过控制旋转床转速实现的,在高转速的情况下,可以达到提高浆液表面更新率,强化传质过程的效果,因此高浓度浆液得以搅拌充分,有效地防止了氢氧化钙原料过度包覆的可能,以此提供了一个相对普通重力场更合适的球钙生成环境,也可以解释在超重力因子相对较低时球形度并不理想的现象,而当超重力因子过高时,离心力过大,会将成型的球形碳酸钙进行物理破坏,使其无法形成完整的球体。在整个碳化反应过程中,体系初始反应的pH为11~12,分别在pH为10、9、8、7时(对应碳化反应时间为5min、7min、9min和12min)取样并进行红外分析得到红外谱图,如图10所示。分析图10可知,所取的四个样品中均存在L-谷氨酸,在整个碳化反应过程中,pH为10时的样品谱图在2514cm-1出现了羧基二聚体吸收峰,可以证明L-谷氨酸发生了解离并且与钙离子发生了静电吸引结合在一起,而并非单纯地附着在碳酸钙表面,此时溶液中存在少量碳酸钙和L-谷氨酸中间体。而随着pH的不断降低,即随着碳化反应的不断进行,羧基二聚体的吸收峰不断减弱。当反应达到终点(pH=7)时,羧基二聚体的吸收峰消失。证明L-谷氨酸中间体消失,反应结束。即在反应初期,L-谷氨酸与溶液中游离的钙离子结合为羧基二聚体(L-谷氨酸水解带一价负电,钙离子带二价正电,一个钙离子与两个谷氨酸结合)。该中间体作为晶种模板引导碳酸钙的形成,随着反应的进行,中间体的数量逐渐减少,在红外中显示为2514cm-1处峰强度不断减弱。至pH=7时,中间体消失,溶液中的钙离子完全转化为碳酸钙,在红外谱图中表现为2514cm-1处的吸收峰消失。L-谷氨酸中间体结构如图11所示。不同pH下取得的样品进行XRD分析,实验结果如图12所示。由图12可知,当反应体系pH为10、9、8时,因反应尚未结束,因此体系中仍然存在氢氧化钙衍射峰。当pH为8时,氢氧化钙衍射峰极弱,说明反应接近结束。至pH=7时,氢氧化钙衍射峰消失,生成球霰石型碳酸钙。可以看到随着碳化反应的进行,反应体系中并未出现方解石,而是始终以球霰石的形式进行生长,而当溶液体系中不含有NH4+时,将会生成方解石与球霰石共存的产物,说明反应体系中NH4+的存在确实能够对方解石的形成进行抑制,并且在NH4+大量存在的环境中,球霰石并未发生溶解-重结晶过程,发生晶型转变成为热力学上更稳定的方解石,证明NH4+的存在能够稳定球霰石。反应开始前,体系中的L-谷氨酸在碱性条件下发生水解,通过静电作用与钙离子结合成为晶种模板,随着气体的通入,二氧化碳溶解在体系中成为碳酸根离子,并在晶种模板的引导下与钙离子结合生长成为碳酸钙,而后体系中大量存在的铵根离子控制碳酸钙晶型向着球霰石型碳酸钙转变,这一晶型的碳酸钙在L-谷氨酸的修饰下成长为球形。使用超重力反应结晶碳化法,以L-谷氨酸与氯化铵为添加剂,制得了粒径均一、晶型为球霰石的球形碳酸钙。分别探讨了L-谷氨酸与氯化铵添加量、超重力水平大小对产物晶型和球形度的影响。结果显示,在L-谷氨酸与氯化铵添加量分别为氢氧化钙4%和20%、超重力因子为161.0的最优条件下,可以制得粒径约为500nm、球形度较高的纯球霰石碳酸钙。探明了各影响因素对球霰石碳酸钙形成的机理:反应开始前,L-谷氨酸与溶液中钙离子形成模板影响了碳酸钙的成核与生长,反应进程中溶液中大量存在的NH4+给球霰石的形成提供了一个良好的环境,超重力反应器对液体的高速切割防止了氢氧化钙原料过度包覆的可能,实现了球形碳酸钙的可控制备。